Was bedeutet BioVAT-HF?
BioVAT-HF steht für Biological Ventricular Assist Tissue in terminal Heart Failure: Die Studie untersucht, unter welchen Bedingungen künstliches Herzgewebe, auch als Herzpflaster bezeichnet, in der Behandlung von Patient*innen mit schwerer Herzschwäche sicher und wirksam eingesetzt werden kann.
Wie werden Herzpflaster hergestellt?
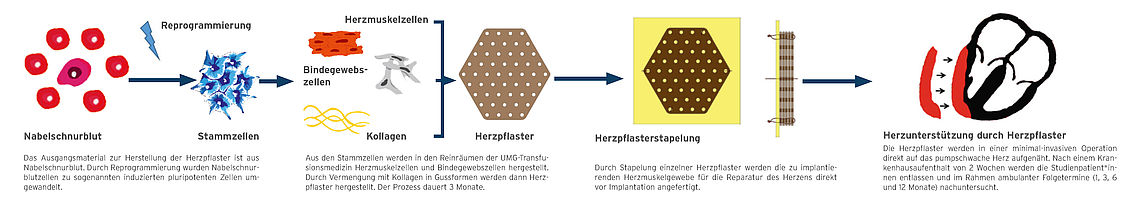
Herzpflaster werden über ein am Institut für Pharmakologie und Toxikologie der Universitätsmedizin Göttingen entwickeltes Verfahren hergestellt. Dafür werden aus sogenannten induzierten pluripotenten Stammzellen Herzmuskelzellen und Bindegewebszellen gewonnen und mit Kollagen in Gussformen vermengt. Die so gezüchteten Herzpflaster zeigen Eigenschaften von jugendlichem Herzmuskelgewebe. Nach einem 3-monatigen Herstellungsprozess in zertifizierten Reinräumen der Transfusionsmedizin der Universitätsmedizin Göttingen werden die Herzpflaster für die Implantation freigegeben.
Für wen kann die Implantation eines Herzpflasters nützlich sein?
Patient*innen mit Herzmuskelschwäche haben im Rahmen ihrer Erkrankung Herzmuskelzellen unwiderruflich verloren. Durch den Schutz des schwachen Herzens über Medikamente kann der Verlauf der Erkrankung verlangsamt werden. Ein Ausgleich des verloren gegangenen Herzmuskels wird nicht erreicht. In späten Stadien der Erkrankung bleiben die Implantation von sogenannten Herzpumpen oder die Herztransplantation als letzte Therapieoptionen. Im Rahmen der BioVAT-HF Studie wollen wir prüfen, ob sich das defekte Herz in Patient*innen mit einer schweren Herzmuskelschwäche trotz optimaler Behandlung reparieren lässt. Studienpatient*innen haben eine stark eingeschränkte Herzpumpfunktion (Auswurfsfraktion ≤35%) und zeigen Krankheitssymptome bereits bei alltäglicher Belastung.
Was passiert während der Studie und wie ist der Ablauf?
Nach Aufklärung und Einwilligung werden Studienpatient*innen einer umfassenden Untersuchung des aktuellen Gesundheitszustandes unterzogen. Unter Berücksichtigung der erhobenen Befunde durch die Prüfärzte aus der Kardiologie und Herzchirurgie wird der operative Eingriff für die Herzpflasterimplantation individuell geplant. Etwa eine Woche vor der Herzpflasterimplantation müssen die Studienpatient* innen mit der Einnahme von Immunsystem hemmenden Arzneimitteln beginnen. Dies ist notwendig, damit das Herzpflaster nach Implantation nicht abgestoßen wird.
Die Studienpatient*innen werden einen Tag vor der Herzpflasterimplantation stationär aufgenommen. Am Folgetag werden die Herzpflaster implantiert. Dies erfolgt über einen minimal-invasiven Zugang, d.h. über einen etwa 5 cm großen Schnitt auf der linken Seite des Brustkorbs direkt auf das schlagende Herz. Das Herzpflaster wird direkt auf dem zuvor diagnostisch gesicherten Herzmuskeldefekt aufgenäht. Das operative Vorgehen gleicht der Fixierung von Herzschrittmacherkabeln auf dem Herzen und dauert von der Einleitung bis Ausleitung der Vollnarkose etwa 90 Minuten. Nach Herzpflasterimplantation bleiben Studienpatient*innen für zwei Wochen im behandelnden Klinikum zur Überwachung und werden dann in die ambulante Betreuung entlassen. Im Rahmen von umfangreichen Folgeuntersuchungen 1, 3, 6 und 12 Monate nach Implantation wird der therapeutische Effekt des Herzpflasterimplantats überprüft. Bei dem Nachweis eines Behandlungserfolgs nach 12 Monaten empfehlen wir eine Weiterführung der Behandlung im Rahmen der Routineversorgung mit Fortsetzung der Immunsuppression. Stellt sich kein Behandlungserfolg ein, wird ein Absetzen der Immunsuppression empfohlen. Studienpatient*innen werden über den gesamten Zeitraum der Studie über die Herzinsuffizienz-Ambulanzen der beteiligten Studienzentren in enger Abstimmung mit Hausärzt*innen bzw. niedergelassenen Kardiolog*innen betreut.
Entstehen Kosten durch die Teilnahme?
Durch Ihre Teilnahme an dieser klinischen Prüfung entstehen für Sie keine zusätzlichen Kosten. Die stationäre Behandlung inklusive Herzpflasterimplantation sowie die Verabreichung der Immunsuppression werden durch das Deutsche Zentrum für Herz-Kreislauf-Forschung (DZHK) und die Repairon GmbH getragen.
BIOVAT-HF-DZHK20 Herzpflaster